燃料电池氢气的几种制造方法
氢气不仅是重要的工业原料和还原剂,也是燃料电池的必要燃料。随着燃料电池的推广和普及,燃料电池汽车进入成熟市场,氢的消耗量也会以惊人的速度增加。目前工业制氢主要有几种方法:
采用化石燃料制取氢气;
从化工副产物中提取氢气;
采用来自生物的甲醇甲烷制取氢气;
利用太阳能、风能等自然能量进行水的电解。
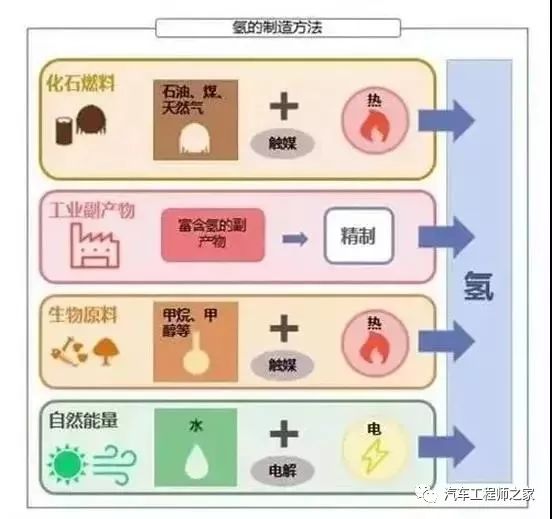
氢气制造方法
化石燃料制氢
化石燃料制氢是比较传统的制氢方法,也是制氢的老工艺,但仍然离不开对化石燃料的依赖,并且会排出二氧化碳等温室气体,导致燃料电池环保价值降低。一般用于制氢的化石燃料为天然气。天然气制氢的过程是:在一定的压力和高温及催化剂作用下,天然气中烷烃和水蒸汽发生化学反应。转化气经过沸锅换热、进人变换炉使C0变换成H2和CO2。再经过换热、冷凝、汽水分离,通过程序控制将气体依序通过装有3种特定吸附剂的吸附塔,由变压吸附(PSA)升压吸附N2、CO、CH4、CO2,提取产品氢气。
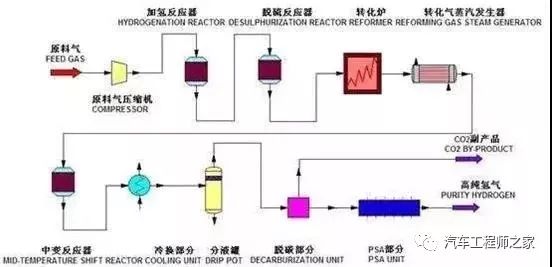
天然气制氢原理
焦炉气制氢
焦炉气制氢技术是采用变压吸附的工艺,从炼焦行业副产的焦炉气中提取纯氢。其基本原理是利用固体吸附剂对气体的吸附具有选择性,以及气体在吸附剂上的吸附量随其分压的降低而减少的特性,实现气体混合物的分离和吸附剂的再生,达到提纯制氢的目的。
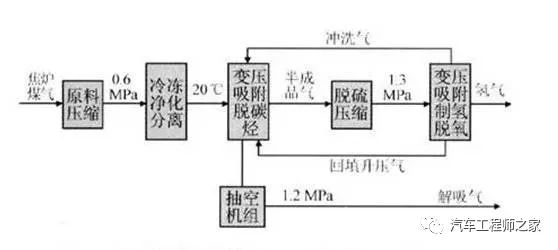
焦炉气制氢原理
甲醇裂解制氢
甲醇裂解制氢的工艺过程是甲醇和除盐水按一定的配比混合,加热至270℃左右的混合物蒸汽,在催化剂(Cu-Zn-Al)或者(Cu-Zn-Cr)的作用下,发生催化裂解和转化反应。
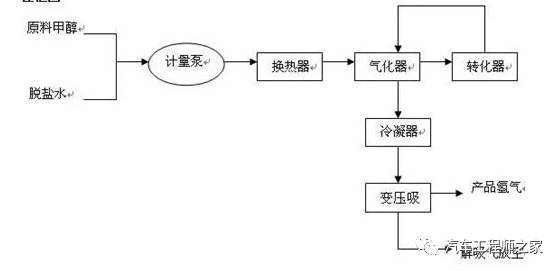
甲醇裂解制氢原理
电解水制氢
氢气还能够通过传统的电解水法获得,但这种方法由于能耗过高,除已建成装置外,已少有新建装置。
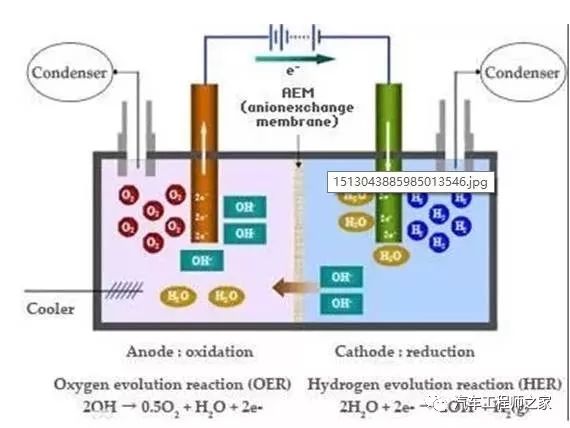
电解水制氢
有上述各方法可知,在工业上目前已经有多种制氢的途径。这些方法都有各自的优势和局限性。天然气制氢和焦炉气制氢均适用于大规模制氢,但也均受限于原料的供应,并且具有污染性。在环保方面,焦炉气制氢利用的虽然是炼焦的副产物,但无法去除其中的污染物,而天然气制氢依然需要化石燃料作为原料。相比之下,甲醇裂解制氢具有投资低、建成快、无污染等特点,并且甲醇作为原料可以更为灵活,但甲醇裂解制氢难以进行大规模的制氢。
从经济性上看,制氢的成本很大程度上取决于原料的成本,随原料价格的波动非常明显。就目前的原料价格水平看,焦炉气制氢和天然气制氢成本更低。
综合目前工业制氢方式的优劣势及成本考虑,如果用氢装置附近有丰富的焦炉气资源,焦炉气制氢技术是首选的工艺技术方案。考虑到制氢规模的要求,天然气制氢技术在能够取得天然气资源的情况下也是优选的方案。甲醇裂解制氢的成本波动性大,制氢规模小,但装置成本低,因此适用于间断性、补充性的氢气制造。
LiTFSI作为电解液添加剂表现出优异性能
新能源Leader 凭栏眺
目前商业锂离子电池电解液的锂盐主要是LiPF6,LiPF6赋予了电解液优异的电化学性能,但是LiPF6的热稳定和化学稳定性比较差,并且对水分非常敏感,在少量H2O的作用下会分解产生HF等酸性物质,进而腐蚀正极材料导致过渡金属元素溶解,并迁移到负极的表面,破坏SEI膜,导致SEI膜持续生长,从而导致锂离子电池的容量持续衰降。
为了克服这些问题,人们曾寄希望于对H2O更加稳定,并且具有更好的热稳定和化学稳定性的酰亚胺类锂盐,例如LiTFSI、LiFSI和LiFTFSI等锂盐,但是受到成本因素的限制,以及无法解决LiTFSI等锂盐的阴离子对Al箔的腐蚀等问题,LiTFSI锂盐一直没有在实际中应用。近日,德国HIU实验室的Varvara Sharova等为酰亚胺类锂盐的应用找到了新的出路——作为电解液添加剂。
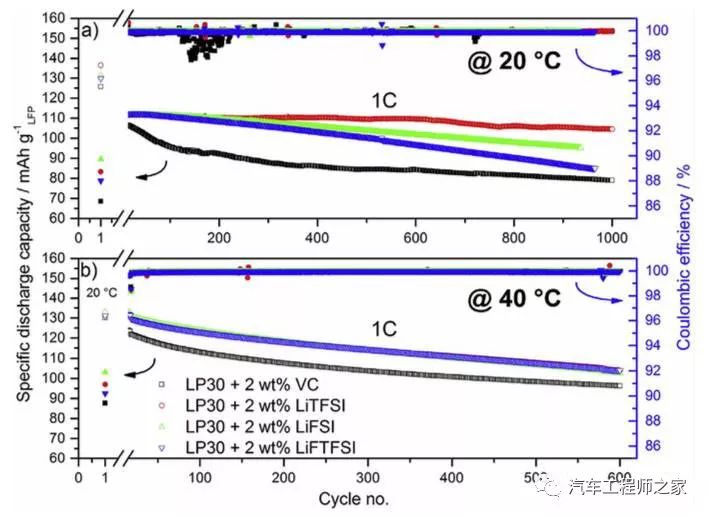
锂离子电池石墨负极的电势比较低,会导致电解液在其表面发生分解,形成钝化层,也就是我们常说的SEI膜。SEI膜能够防止电解液继续在负极表面发生分解,因此SEI膜的稳定性对于锂离子电池的循环稳定性有着至关重要的影响。虽然LiTFSI等锂盐暂时还无法作为商业电解液的溶质使用,但是作为添加剂使用时却起到了非常好的效果。Varvara Sharova的实验发现,在电解液中添加2wt%的LiTFSI,可以有效的提升LiFePO4/石墨电池的循环性能:20℃下循环600次,容量衰降小于2%,而作为对照组添加2wt%VC添加剂的电解液,同样的条件下,电池容量的衰降达到了20%左右。
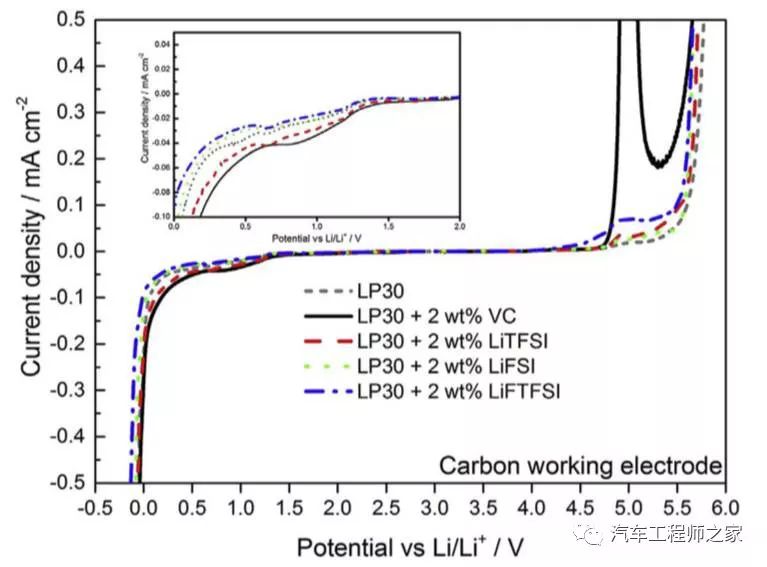
为了验证不同添加剂对锂离子电池性能的影响,Varvara Sharova分别制备没有添加剂的空白组LP30(EC:DMC=1:1)和添加VC、LiTFSI、LiFSI和LiFTFSI的实验组电解液,并利用扣式半电池和全电池对这些电解液的性能进行了评估。
上图为空白对照组与实验组电解液的伏安曲线,在还原的过程中,我们注意到空白组电解液在0.65V左右出现了一个明显的电流峰,对应的是EC溶剂的还原分解,添加VC添加剂的实验组电解液的分解电流峰向高电势处发生了偏移,这主要是因为VC添加剂的分解电压高于EC,因此首先发生了分解,对EC形成了保护。而添加LiTFSI、LiFSI和LiFTFSI添加剂的电解液的伏安曲线与空白组没有明显的区别,这说明酰亚胺类的添加剂并不能减少EC溶剂的分解。
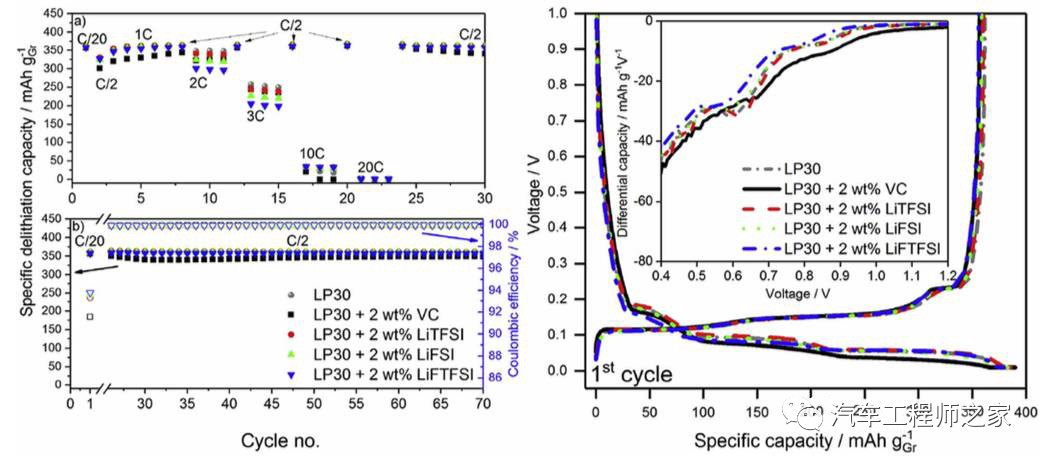
上图为石墨负极在不同的电解液中的电化学性能,从首次充放电的效率来看,空白组的首次充放电库伦效率为93.3%,添加LiTFSI、LiFSI和LiFTFSI的电解液的首次效率分别为93.3%、93.6%和93.8%,但是添加VC添加剂的电解液的首次效率仅为91.5%,这主要是因为在石墨首次嵌锂过程中,VC在石墨负极的表面发生分解消耗了较多的Li。
SEI膜的成分会对离子电导率产生较大的影响,进而影响锂离子电池的倍率性能,在倍率性能测试中发现,采用LiFSI和LiFTFSI添加剂的电解液,在大电流放电时容量发挥稍低于其他电解液。在C/2循环测试中,所有添加酰亚胺类电解液循环性能非常稳定,而添加VC添加剂的电解液出现了容量衰降的现象。
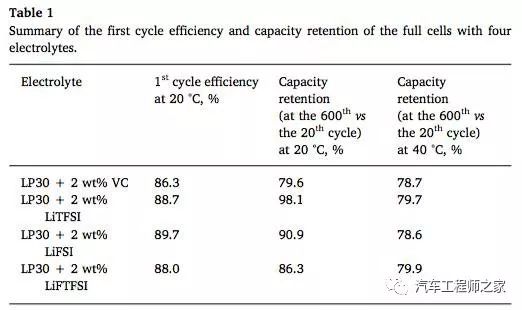
为了评估电解液在锂离子电池长期循环中的稳定性,Varvara Sharova还利用扣式电池制备了LiFePO4/石墨全电池,对添加不同添加剂的电解液在20℃和40℃下的循环性能进行了评估,下表为评估结果。从表中可以看到添加LiTFSI添加剂的电解液不仅首次效率要明显高于添加VC添加剂的电解液,在20℃下的循环性能更是具有压倒性的优势,循环600次添加LiTFSI的电解液容量保持率为98.1%,而添加VC添加剂的电解液的容量保持率仅为79.6%。但是在40℃度下循环时,这样的优势就消失了,所有的电解液都具有相近的循环性能。
从上面的分析,我们不难看出酰亚胺类锂盐作为电解液添加剂时能够显著的提升锂离子电池的循环性能。为了研究LiTFSI等添加剂在锂离子电池内的作用机理,Varvara Sharova利用XPS对石墨负极在不同的电解液中形成的SEI膜成分进行了分析,下图为在第1次和第50次循环后,石墨负极表面形成的SEI膜的XPS分析结果。可以看到在添加LiTFSI添加剂的电解液中形成的SEI膜中LiF的成分含量要明显高于添加VC添加剂的电解液。进一步对SEI膜的成分进行定量分析表明,在第1次循环后,SEI膜中LiF含量的高低顺序为LiFSI>LiFTFSI>LiTFSI>VC>空白组,但是SEI膜在首次充电的过程中形成后并不是一成不变的。随着电池的循环,SEI膜的成分也在不断发生的变化,在经过50次循环后,LiFSI和LiFTFSI电解液中的SEI膜中的LiF成分分别下降了12%和43%,而添加LiTFSI的电解液中的LiF成分反而增加了9%。
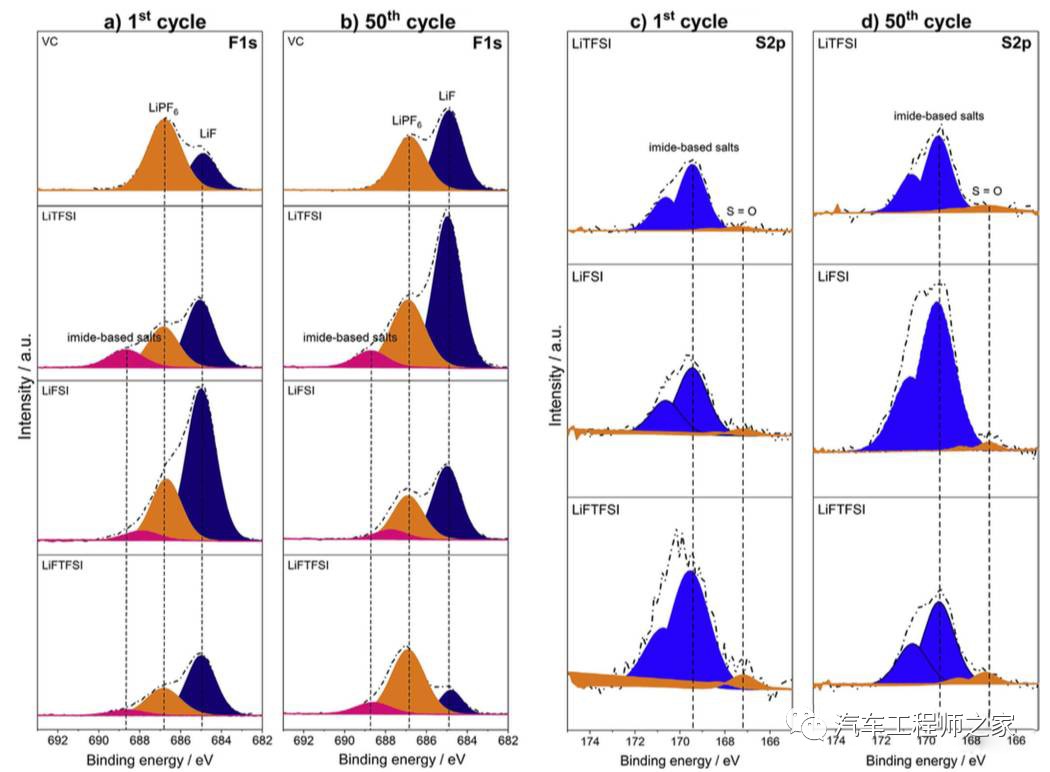
一般我们认为SEI膜的结构分为两层:内层无机层和外层的有机层,无机层主要是由LiF、Li2CO3等无机成分组成,它们的电化学性能更佳稳定、离子电导率更高,外层的有机层主要由多孔的电解液分解和聚合产物组成,如ROCO2Li、PEO等组成,对电解液的保护能力不强,因此我们希望SEI膜中的无机成分更多一些。酰亚胺类添加剂能够为SEI膜带来更过的无机LiF成分,从而使得SEI膜的结构更加稳定,能够更好的防止电解液在电池循环过程中发生分解,减少Li的消耗,从而显著的提升电池的循环性能。
酰亚胺类锂盐在作为电解液添加剂,特别是LiTFSI添加剂能够显著的改善电池的循环性能,这主要是得益于添加LiTFSI后,石墨负极表面形成的SEI膜的LiF更多,SEI膜更薄也更稳定,从而减少了电解液的分解、降低了界面电阻。但是从目前的实验数据来看,LiTFSI添加剂更加适合在常温下使用,在40℃的高温下,LiTFSI添加剂相比于VC添加剂没有明显的优势。














获取更多评论